P07 - Thomas Stamminger
Kontrollmechanismen des transkriptionellen silencing während der Cytomegalievirus-Infektion
- Humanes Cytomegalievirus (HCMV)
- Silencing-Faktoren
- Repressorbesetzung des viralen Genoms
- Transkriptionelle Charakteristiken, die die Silencing-Funktion bestimmen
- Visualisierung des silencing des viralen Genoms
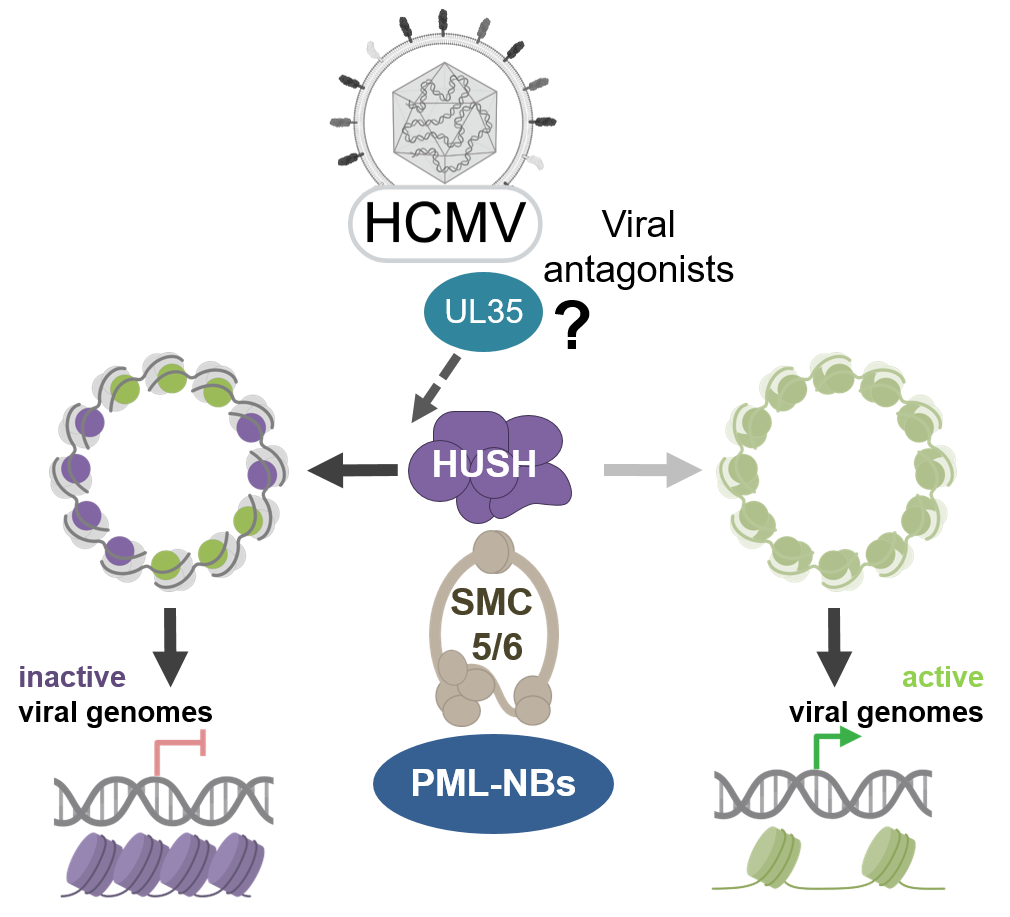
Das humane Cytomegalievirus (HCMV), ein extrem speziespezifisches Herpesvirus, hat eine Vielzahl von Mechanismen entwickelt, um die Wirtsabwehr zu unterlaufen, was letztlich zu einer lebenslangen viralen Persistenz führt. Jüngste Studien deuten darauf hin, dass zelleigene Restriktionsmechanismen wie PML nuclear bodies (PML-NBs) eine entscheidende Rolle für die Quieszenz des HCMV spielen. Auf der Grundlage von Ergebnissen, die in einem gemeinsamen Ansatz während des ersten Förderzeitraums erzielt wurden, soll die Rolle von zwei neuen PML-assoziierten Repressorkomplexen, SMC5/6 und HUSH, für die HCMV-Replikation zu untersuchen. Der SMC5/6-Komplex (Structural Maintenance of Chromosomes) spielt eine zentrale Rolle bei der DNA-Reparatur, wirkt aber auch antiviral, indem er zirkuläre extrachromosomale DNA kompaktiert. Für HUSH (Human Silencing Hub) wurden kürzlich zwei paraloge Komplexe beschrieben. HUSH1 soll LINE-1-Retrotransposons reprimieren, während HUSH2 bevorzugt interferon-stimulierte Gene reguliert. Wir vermuten eine Doppelrolle von SMC5/6 und HUSH während der HCMV-Infektion. Zu Beginn der HCMV-Transkription könnten diese Komplexe eine repressive Wirkung haben, die durch das Virus antagonisiert werden muss. Der lange Replikationszyklus von HCMV könnte jedoch die Nutzung von Komponenten dieser Mechanismen in späteren Phasen der Infektion erforderlich machen. Im Einklang mit der Antagonisierung der Repression haben wir eine starke Hochregulierung von transposable elements (TEs) wie LINE-1 sehr früh während der HCMV-Infektion beobachtet. Das Projekt verfolgt daher drei Hauptziele: (i) Identifizierung der viralen Proteine und der Mechanismen, die zur Antagonisierung der repressiven Funktionen von HUSH und SMC5/6 verwendet werden; (ii) Charakterisierung der Funktionen von HUSH- und SMC5/6-Komponenten, die in späteren Phasen der HCMV-Replikation benötigt werden; (iii) Klärung der Rolle von HUSH und anderen regulatorischen Faktoren bei der Modulation von TEs während der HCMV-Infektion. Wir werden diese Proteinkomplexe in einer hochgradig interaktiven und vergleichenden Weise zusammen mit anderen DEEP-DV-Mitgliedern untersuchen. Dies soll neue mechanistische Erkenntnisse über die Rolle dieser molekularen Maschinerien für die lytische Replikation und Persistenz von DNA-Viren liefern.


