P03 - Markus Landthaler
RNA-vermittelte Regulation der Transkription während einer Herpes simplex virus 1 Infektion
- Regulation der Transkription
- Herpes Simplex Virus 1
- Protein-RNA Interaktionen
- Die Rolle von RNA-bindenden Proteinen bei Virusinfektionen
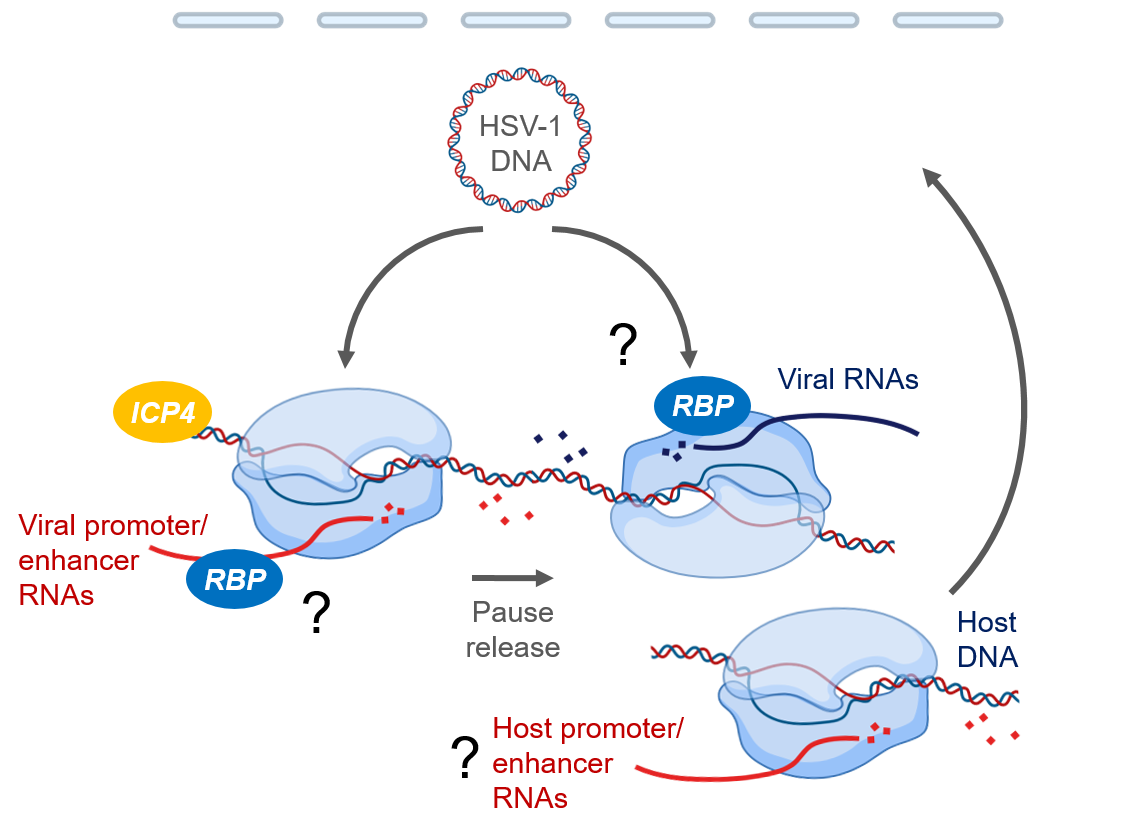
Das Herpes-Simplex-Virus Typ 1 (HSV-1) hat ein Genom aus doppelsträngiger DNA, repliziert im Zellkern menschlicher Zellen und benötigt eine große Zahl von Faktoren der Wirtszelle für die Transkription und Prozessierung seiner RNAs. RNA-bindende Proteine (RBPs) und nicht-codierende RNAs wie bspw. Enhancer-RNAs (eRNAs) und lange nicht-codierende RNAs (lncRNAs) beeinflussen these Prozesse auf verschiebenen Ebenen – von der Rekrutierung von Transkriptionsfaktoren über Chromatin-Modellierung, Initiation der RNA-Polymerase II bis zur promoter-proximalen Pausierung und der Ablösung davon. In diesem Projekt untersuchen wir, wie Protein-RNA-Interaktionen die Transkription und Produkte in HSV-1-Infektionen steuern. Interessanterweise haben wir entdeckt, dass der virale Transkriptionsfaktor ICP4 von HSV-1 auch direkt mit RNA interagiert ist. Um die Funktion der Wirts-RBPs direkt zu untersuchen, haben wir HCT116 Degron-Zellen so präpariert, dass eine Reihe von Proteinen mit RNA-Bindungsaktivität, die am proximalen Pausieren des Promotors, der Ablösung davon und der Transkriptions-Elongation beteiligt sind, sowie nukleäre RBPs, die zuvor als relevant bei HSV-1-Infektionen identifiziert wurden, schnell entfernt werden. Auf der Grundlage unserer vorläufigen Daten sollen in diesem Verbundprojekt die molekularen RNA-basierten Mechanismen der HSV-1-Transkription systematisch untersucht werden. Das Projekt verfolgt drei Hauptziele: (i) Charakterisierung der ICP4-Domänenstruktur und relevanter RNA-Interaktionen bei der frühen Transkription von HSV-1-Infektionen, (ii) Funktionsanalyse von RBPs, die an der Transkriptionsinitiierung und -verlängerung beteiligt sind, und (iii) Untersuchung der Rolle von Enhancer-RNAs bei der Regulierung des Transkriptionsprogramms von HSV-1-infizierten Zellen. Zusammenfassend lässt sich sagen, dass dieses Projekt unser Verständnis der frühen HSV-1-Transkriptionsereignisse erheblich verbessern wird und das Potenzial für die Anwendung von Antisense-Oligonukleotiden zur sequenzspezifischen Beeinflussung der RNA-Funktion als neuartiger therapeutischer Ansatz bietet.


